破解工业菌株开发难题:十大核心策略与实践指南

引言
系统代谢工程
为什么许多在实验室表现优异的微生物菌株,难以在工业生产中落地?传统菌株开发为何耗时耗力?2015年,韩国科学技术院Sang Yup Lee团队Nature Biotechnolog 发表的综述《Systems strategies for developing industrial microbial strains》,给出了系统性答案。今天,我们用一篇文章,为你梳理其中的核心思想,看看如何用“系统代谢工程”的策略,打通从实验室到工厂的“最后一公里”。

行业痛点:传统菌株开发的“三重困境”
工业微生物菌株开发的目标是通过全系统工程改造细胞代谢,实现目标产物的高效合成,同时兼顾发酵、分离纯化等工业工艺。然而,当前行业面临三大核心挑战:
1.网络复杂性:细胞内代谢网络、基因调控网络与信号传导网络相互作用极为复杂,难以厘清其协同效应;
2.开发成本高:传统方法需耗费50-300人/年工作量及数亿美元投资;
3.转化成功率低:学术研究成果向工业转化的成功率极低,核心原因在于:
学术研究常聚焦于菌株本身改造,忽视完整工业生物工艺流程的系统性;
企业在采纳前沿代谢工程技术方面滞后于学术界。
破局关键:产学研深度协作+ 系统代谢工程框架(整合系统生物学、合成生物学与进化工程)。
系统代谢工程:从“单点改造”到“全局优化”
自1991年代谢工程正式确立以来,已从传统的单基因改造演进为“系统代谢工程”。该框架将上游(菌株开发)、中游(发酵)、下游(分离纯化)视为有机整体,通过多学科技术整合,已实现多项突破:
1.效率提升:仅需10人年即可开发出高产L-缬氨酸、L-苏氨酸的大肠杆菌菌株,较传统方法大幅缩短周期;
2.产品拓展:成功构建高产1,4-丁二醇、青蒿素、琥珀酸等产物的工业菌株。
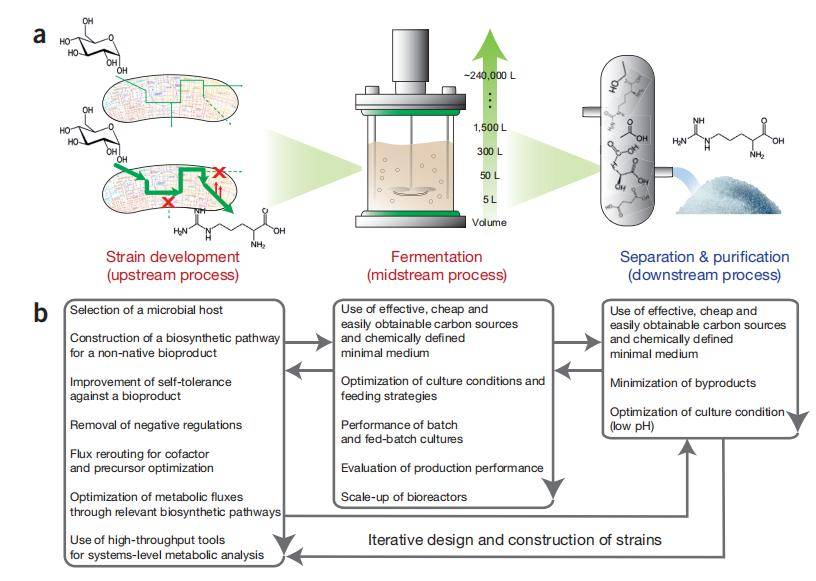
系统代谢工程框架概念。(a)3个主要的生物流程阶段:上游阶段-菌株开发、中游阶段-发酵和下游阶段-分离和纯化(b)系统代谢工程中优化生物工艺全流程的考量因素。菌株开发和发酵的优化有助于提高微生物菌株的生产性能(红色),而分离和纯化的优化则通过促进下游工艺帮助降低整体运营成本(蓝色)。部分因素在系统代谢工程过程中会重复出现。
十大核心策略:教你开发“六边形战士”菌株
文章探讨了基于系统代谢工程视角工业微生物菌株开发成功案例的十种通用策略。
1.项目设计——明确“目标-指标-可行性”
立项之初,就要站在整个工艺流程的角度,问自己几个问题:目标产物是什么?浓度、产率要达到多少才有竞争力?用现有技术做,成本能打下来吗?这一步的技术经济分析,是学术界最容易忽略,但对产业化却至关重要的一环。
2.宿主菌株选择——“天然潜力+可操作性+工艺兼容性”
是选大肠杆菌、酵母这类“熟门熟路”的模式菌株,还是选某些有天然潜力的“小众菌株”(如产琥珀酸曼海姆菌)?决策的关键在于:遗传操作是否方便、是否适合目标产物、是否适应工业发酵的粗放环境。
3.代谢途径重构——构建非天然产物合成路径
针对宿主中不存在的目标产物合成途径,需通过“基因挖掘-异源表达-优化适配”三个步骤来进行构建优化。直至文章发表的15年,除了大规模平行实验外,尚无简便方法缩短开发最优合成途径所需时间,这一步骤成为途径设计的瓶颈。但小编认为随着近几年AI工具如AlphaFold等模型的发展和完善,“干湿”实验的结合有望实现这一步骤的技术突破。
4.提高产物耐受性——解除代谢通量限制
产物积累易对宿主产生毒性抑制,需通过“耐受性改造”解除限制,这一过程可在菌株开发任一阶段实施。常用改造方法包括:
进化工程:逐步提高产物浓度,筛选生长更快的耐受菌株;
理性设计:改造外排泵、调控膜梯度(如大肠杆菌中过表达L-缬氨酸外排泵,产物滴度提升40%以上)。
5.去除负调控回路——突破“合成瓶颈”
细胞经长期进化形成负反馈回路(如转录衰减、反馈抑制),普遍存在于微生物细胞中,需通过工程改造解除:
转录衰减调控:敲除抑制性调控基因,或用组成型启动子替换天然启动子;
反馈抑制解除:已知抑制位点时定点突变,未知时结合耐受性诱变与基因组测序筛选突变体。
6.重定向代谢通量——优化辅因子和前体供应
辅因子(NADH、NADPH、ATP等)和前体供应不足是高产常见瓶颈,改造的核心手段包括基因敲除(删除竞争途径)、基因敲低(针对必需基因)、酶与途径替换(优化辅因子特异性)。通常,辅因子和前体优化比移除途径特异性负调控回路需要更全面的系统方法,因为在前者情况下,必须考虑全局质量、能量和氧化还原平衡。
7.诊断并优化产物合成通量——迭代逼近最优
需在接近工业发酵的条件下(如补料分批培养),系统诊断代谢瓶颈。核心方法是模拟工业生产条件,结合产率、滴度、生产强度指标,利用13C-代谢通量分析、转录组测序等手段系统分析中间菌株的代谢状况,识别并消除通量瓶颈,减少副产物形成,从而最大化目标产物合成通量;每轮改造后验证性能,根据结果设定下一轮目标。
8.诊断并优化培养条件——“底物适配+环境调控”
通过工艺参数优化弥补菌株缺陷,主要包括
底物优化:选择工业级廉价底物(如糖蜜、生物质水解物),或混合底物调控生长速率;
环境参数:优化pH、温度、氧传递速率、补料策略,适配工业发酵模式。
培养基优化:对于工业规模发酵,培养基成本往往比培养基是限定、半限定还是复杂的性质更为重要。
9.全系统基因操作——完成“最后一公里”优化
在前期改造基础上,通过全系统分析挖掘潜在靶点:
核心技术:基因组规模模拟(如OptKnock算法)、高通量基因组工程(MAGE、合成sRNA)、组学整合分析;
应用逻辑:并非仅在最后阶段应用,在中间菌株阶段即可介入,加速优化进程。
10.放大发酵与诊断——解决“放大效应”
实验室菌株需通过中试或示范工厂规模验证:
核心挑战:性能差异(混合、通气条件不同)、菌株稳定性(基因不稳定性导致表型丢失);
解决方案:工艺微调、稳定性强化(染色体整合改造)、污染控制;
关键指标:中试规模的产率、滴度、生产强度需满足工业竞争力且具有高可重复性。
典型案例:策略用得好,成果差不了
文章用三个案例生动展示了这套策略的威力:
案例1(L-精氨酸): 研究人员以谷氨酸棒杆菌为宿主,综合运用了除策略3外的9大策略。通过敲除调控基因、重定向代谢流、优化培养条件等一系列操作,仅用9人年就开发出高性能菌株,且中试表现稳定。

系统代谢工程总体方案及其在谷氨酸棒杆菌L-精氨酸过量生产方向的案例研究
案例2(1,4-丁二醇):这是一个从零开始构建“非天然产物”合成途径的标杆。通过途径重构、敲除竞争途径、基因组规模模型预测等策略,实验室产量超过18g/L,并成功实现了500万磅的商业化生产。
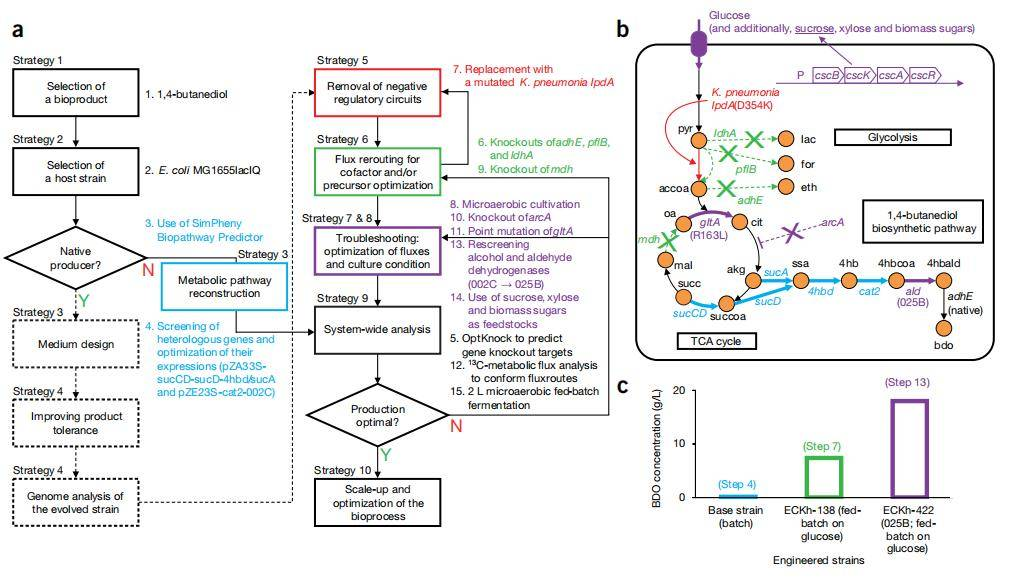
系统代谢工程总体方案及其在大肠杆菌高产1,4-丁二醇的案例研究中的应用示意图
案例3(L-赖氨酸与1,5-二氨基戊烷):这个案例展示了“延伸改造”的潜力。先在谷氨酸棒杆菌中构建了L-赖氨酸的高产菌株(产量达120g/L),然后以其为底盘,通过引入新酶,将L-赖氨酸进一步转化为高价值的尼龙单体——1,5-二氨基戊烷,产量达88g/L。
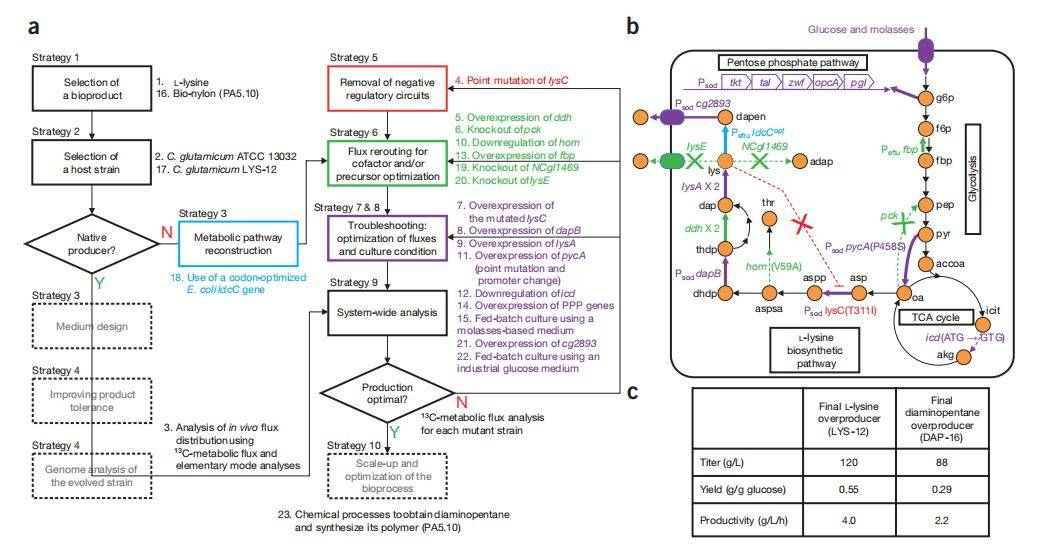
系统代谢工程总体方案及其在利用谷氨酸棒杆菌高产L-赖氨酸和生物尼龙的案例研究
核心挑战
尽管这套系统策略已经大获成功,但我们仍面临诸多挑战:
-
新路不好修:外源基因装进去后,酶活性低,还可能与宿主不合。
-
优化极复杂:如何完美平衡菌株的生长和生产?如何理性设计提高菌株对产物的耐受性?这些都是难题。
-
底物要升级:如何让菌株利用更可持续的原料,如秸秆、餐厨废弃物等,是未来的方向。
-
基础待夯实:我们对细胞代谢网络的理解仍不全面,也缺乏可以“以一敌百”的通用工业底盘菌株。
文章提出的十大系统策略,核心逻辑是“以产品工业化为准则,整合学术界前沿技术,加速菌株与工艺迭代优化”。这些策略的应用成功缩短了菌株开发周期、降低成本,在氨基酸、大宗化学品、药物等多类产物的高效合成与商业化案例中体现出重要指导价值。
泓迅生物作为微生物细胞工厂构建领域的技术赋能者,提供基因“读-写-编”一体化解决方案。从实验室研发到工业化放大,致力于帮助客户跨越“高成本、长周期、低转化率”的行业门槛,加速高价值产物从构想走向商业化。
为什么选择泓迅
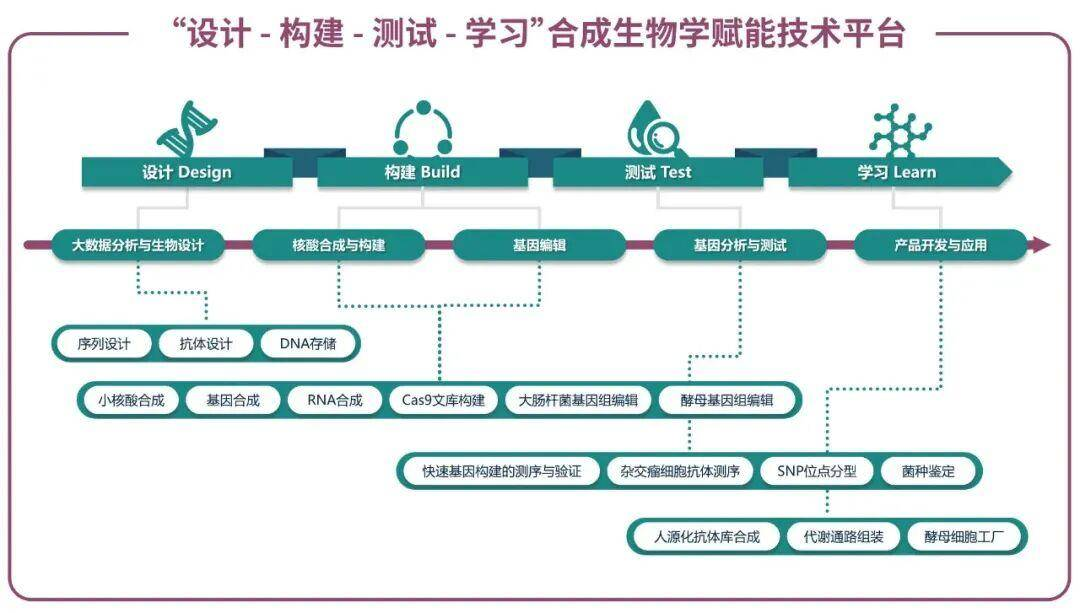
领先的技术优势—AI赋能的合成生物学技术
我们可以做—高难度的序列合成
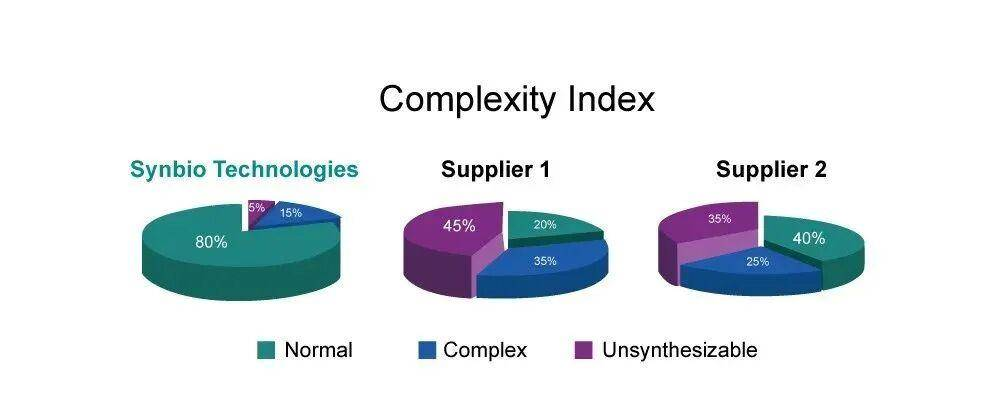
更高的价值服务—一站式生物分子解决方案
 Syno®C 引物合成
Syno®C 引物合成 RNA合成
RNA合成 mRNA合成
mRNA合成 Syno®GS 基因合成
Syno®GS 基因合成 载体构建
载体构建 高通量及DNA文库构建
高通量及DNA文库构建 CRISPR基因编辑平台
CRISPR基因编辑平台 病毒包装
病毒包装 基因测序与组学分析
基因测序与组学分析 重组蛋白表达平台
重组蛋白表达平台 抗体工程平台
抗体工程平台 多肽服务
多肽服务 生物信息学分析与设计
生物信息学分析与设计 CRISPR文库
CRISPR文库 合成生物学产品
合成生物学产品 ProXpress蛋白快速检测
ProXpress蛋白快速检测 CRISPR 质粒
CRISPR 质粒





















