重组胶原蛋白千亿市场背后,还有哪些机会?
从动物组织中提取胶原蛋白具有天然来源、资源丰富以及提取工艺成熟等优势,但面临着对动物资源的依赖性和限制、传染病风险、质量不一等问题。目前,传统提取的方式已无法满足人们对胶原蛋白的巨大需求。
为了避免动物来源胶原蛋白所带来的风险和不确定性, 研究人员采取合成生物制造的策略,利用基因工程技术,选用各种宿主细胞,如植物、昆虫细胞、细菌和酵母等生产重组胶原蛋白或重组胶原蛋白肽。相较动物源胶原蛋白,合成生物制造的重组胶原蛋白具有更高生物相容性、更低免疫原性、更佳的水溶性以及可加工性等优势。
重组胶原蛋白商业化加速研发需求
重组胶原蛋白赛道如火如荼,千亿市场加速研发需求。根据弗若斯特沙利文的预测,中国重组胶原蛋白市场规模将于2024年超过动物源性胶原蛋白;到2027年,中国胶原蛋白市场规模预计会突破1500亿元,其中重组胶原蛋白市场规模将超过1000亿元。
重组胶原蛋白市场正处于快速增长的阶段,其背后的巨大潜力已经吸引了众多企业的关注和投入。然而,随着市场的不断发展和竞争的加剧,仅仅依靠现有的产品和技术难以满足消费者的多元化需求。对于重组胶原蛋白产品的研发,仍然存在许多机会。
近年来,合成生物学飞速发展,DNA测序、DNA合成、DNA编辑和基因表达调控等关键底层技术的进步和成本不断降低,显著提升了我们对胶原蛋白的合成生物制造能力。通过对胶原蛋白DNA的精准操控,在中心法则的框架下,获得可预测、可定量的生物学性状,实现定制化重组胶原蛋白表达及量产优化。这些产品广泛应用于医疗、美容和保健等领域。
|
应用方向
|
用于皮肤修复、口腔修复的生物敷料,骨修复,软骨组织再生等 |
|
多种药物载体的构建 |
|
|
用于面部皱纹和疤痕修复的医美注射填充剂,美白、保湿、抗衰老等护肤产品 |
|
|
水解胶原蛋白作为功能性食品,如咀嚼片、蛋白粉等 |
随着国家政策、产业及资本对重组胶原蛋白领域的聚焦,合成生物学技术成为重组胶原蛋白研发的制胜法宝。目前,部分类型的重组胶原蛋白已成功进行商化业开发与生产,各类相关研究也在日趋深入。
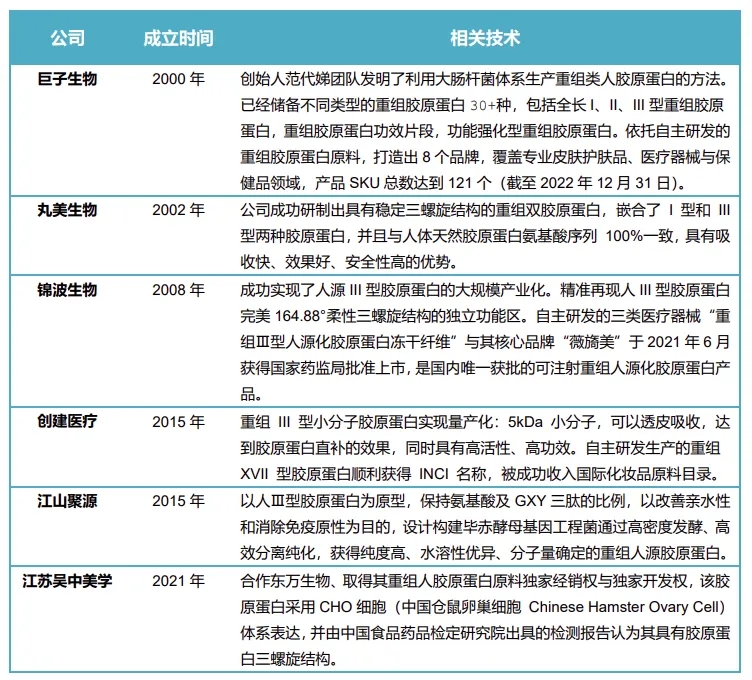
重组胶原蛋白开发过程
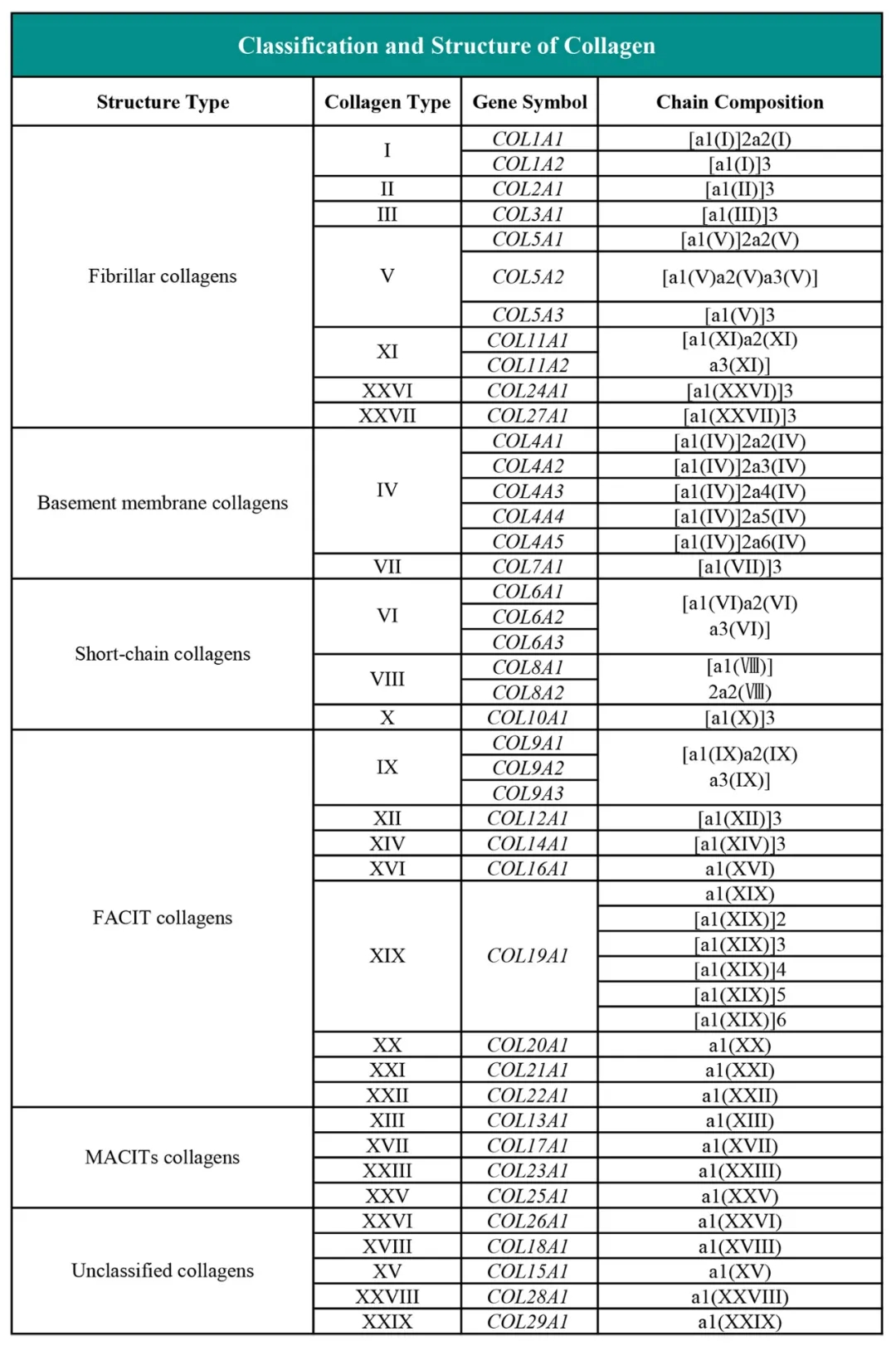
人源胶原蛋白的种类多并结构复杂,目前已发现28种类型,在人体不同的组织器官,全方位参与人体组织器官的修复和再生。其中研究较多的是Ⅰ型、Ⅱ型、Ⅲ型、Ⅵ型、以及XⅢ型胶原蛋白。
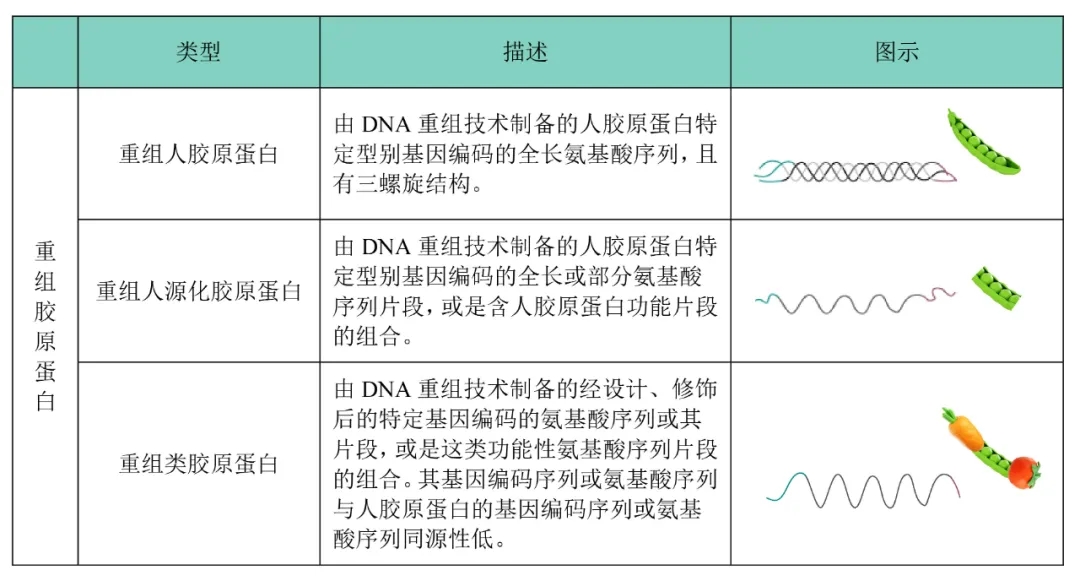
重组胶原蛋白是一种利用DNA重组技术制备的胶原蛋白。在 2021 年 3 月 15 日国家药监局发布的《重组胶原蛋白生物材料命名指导原则》中,将重组胶原蛋白主要分为三类:重组人胶原蛋白、重组人源化胶原蛋白以及重组类胶原蛋白。
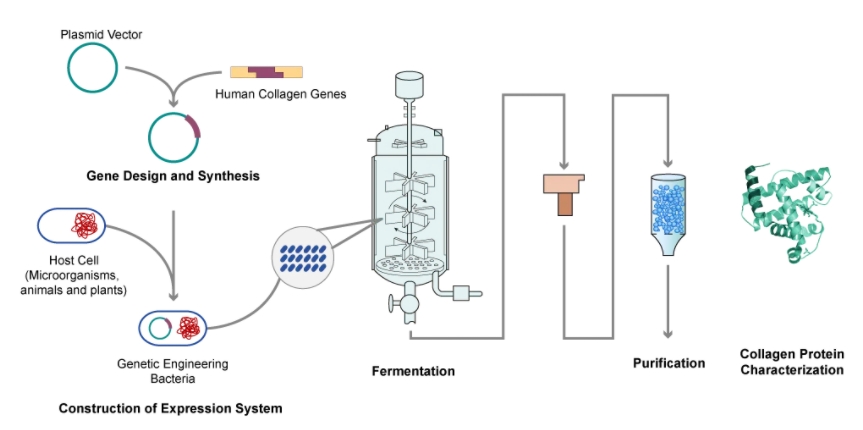
》基因设计与合成:选择要测试的胶原蛋白基因,然后将目标基因克隆到合适的表达载体中。
》构建表达系统:将重组质粒导入合适的宿主细胞(如大肠杆菌、酵母、哺乳动物细胞等)中进行蛋白质表达。在此过程中,宿主细胞在适当的条件下进行培养,以表达目标蛋白质。
》发酵:在发酵过程中,培养基的优化至关重要。培养基中需要提供营养物质,以满足微生物的生长需要。同时,培养条件的控制也非常重要,包括 pH 值、温度、氧气供应等。
》蛋白质纯化: 表达后,需要从宿主细胞裂解物中纯化重组胶原蛋白。这通常涉及一系列纯化步骤,如离心、过滤、层析和沉淀,以从其他杂质中分离和纯化目标蛋白。
》蛋白质表征分析: 最后,对纯化的重组胶原蛋白进行表征,以确认其特性、纯度和生物活性。利用SDS-PAGE、Western 印迹、质谱分析和功能测定等技术评估蛋白质的结构和功能特性。
重组胶原蛋白
合成生物学解决方案
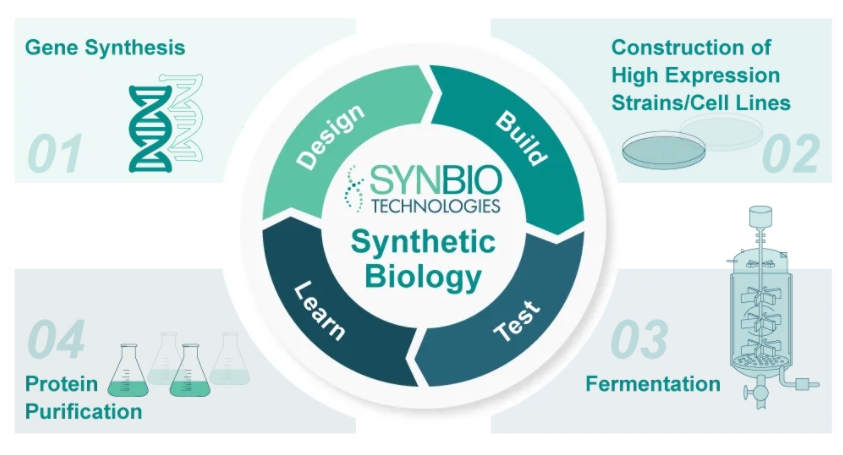
重组胶原蛋白基因的选择和设计、表达条件的优化和验证对于获得高产量的蛋白至关重要。我们提供从“序列优化”到“基因合成”到“重组胶原蛋白表达”一站式服务。高效的基因合成、多种表达体系协助您在实验室低成本无限合成,提高胶原蛋白的表达量、亲水性和可加工性,创造更多应用可能。
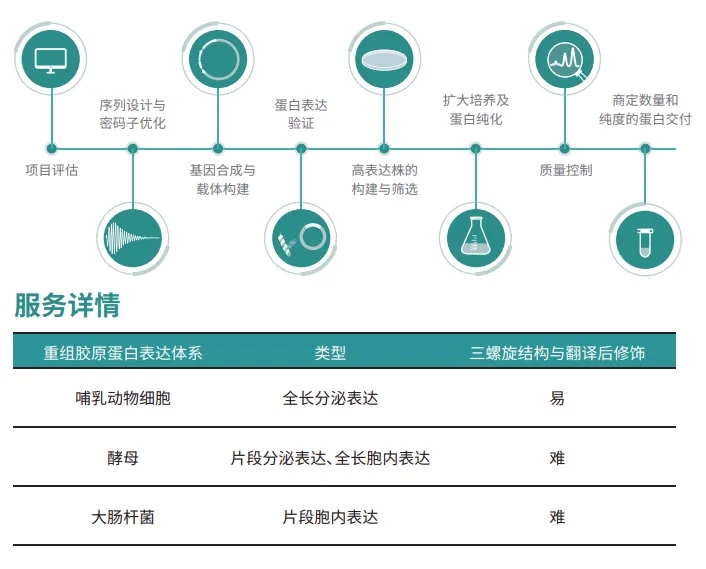
重组胶原蛋白表达服务流程
正确的氨基酸序列对胶原蛋白的功能至关重要,在制备具有特定胶原蛋白序列的三螺旋多肽时,主要技术难点是基因片段的选择及三螺旋结构的稳定性。泓迅生物合成生物学赋能技术平台帮您解决胶原蛋白源头基因合成难点!
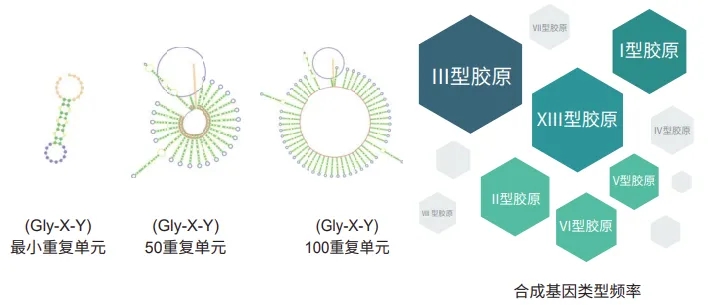
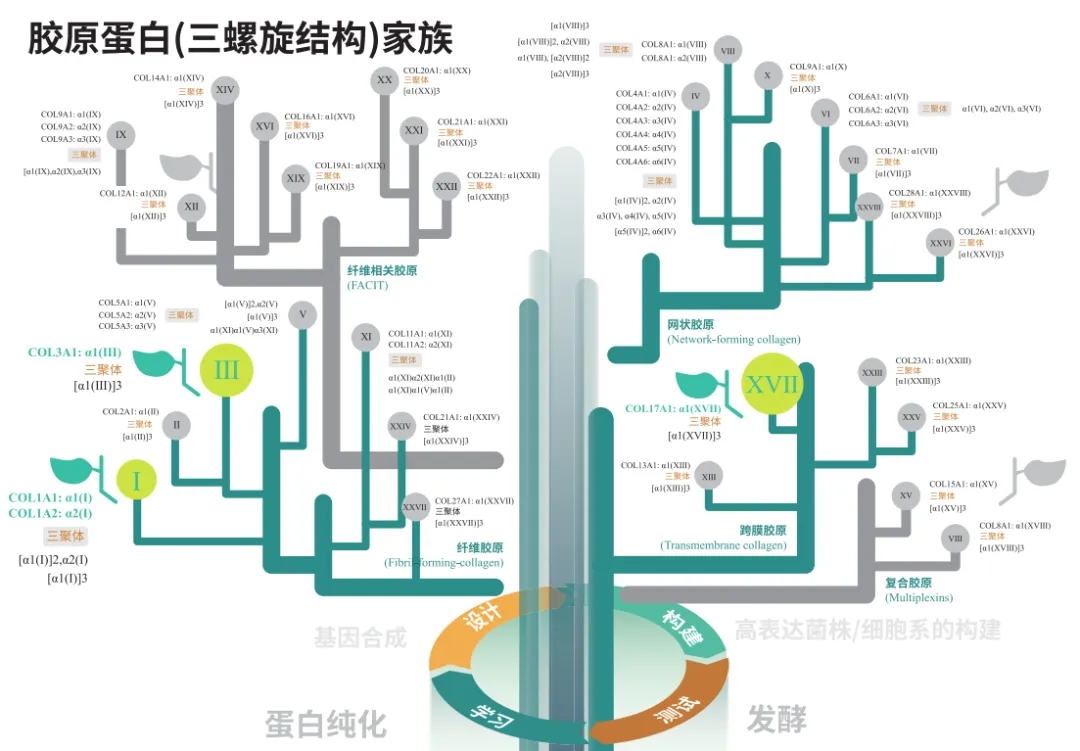
我们在重组胶原蛋白基因合成上拥有丰富经验,精准合成“高”重复基因序列。定制化基因合成设计方案、优质的菌株库与完整的分子克隆工具酶体系,协助您在实验室中低成本尝试大量的基因设计。
Reference:
[1] Yuanyuan ZHANG, Yan ZENG, Qinhong WANG. Advances in synthetic biomanufacturing[J]. Synthetic Biology Journal, 2021, 2(2): 145-160.
[2] Sorushanova A, Delgado LM, Wu Z, Shologu N, Kshirsagar A, Raghunath R, Mullen AM, Bayon Y, Pandit A, Raghunath M, Zeugolis DI. The Collagen Suprafamily: From Biosynthesis to Advanced Biomaterial Development. Adv Mater. 2019 Jan;31(1):e1801651.
[3] Fu R, Fan D, Yang W, Chen L, Qu C, Yang S, Xu L. [Industrial development and biomedical application prospect of recombinant collagen]. Sheng Wu Gong Cheng Xue Bao. 2022 Sep 25;38(9):3228-3242. Chinese.
[4] Zhang YP, Sun J, Ma Y. Biomanufacturing: history and perspective. J Ind Microbiol Biotechnol. 2017 May;44(4-5):773-784.
 Syno®C 引物合成
Syno®C 引物合成 RNA合成
RNA合成 mRNA合成
mRNA合成 Syno®GS 基因合成
Syno®GS 基因合成 载体构建
载体构建 高通量及DNA文库构建
高通量及DNA文库构建 CRISPR基因编辑平台
CRISPR基因编辑平台 病毒包装
病毒包装 基因测序与组学分析
基因测序与组学分析 重组蛋白表达平台
重组蛋白表达平台 抗体工程平台
抗体工程平台 多肽服务
多肽服务 生物信息学分析与设计
生物信息学分析与设计 CRISPR文库
CRISPR文库 合成生物学产品
合成生物学产品 ProXpress蛋白快速检测
ProXpress蛋白快速检测 CRISPR 质粒
CRISPR 质粒





















