人工多酶复合体——打通血红素量产“高速路”

血红素是一种含Fe2+的卟啉类化合物,是高等生物运输氧气、调节机体铁平衡、传递电子和提供能量等方面必需的生化物质。凭借其高效补铁、抗氧化及优异的生物催化活性,血红素在多个关键领域发挥重要作用:
1. 医药领域
-
高效补铁剂: 吸收率高、副作用小,用于治疗缺铁性贫血(保健品/药品)。
-
抗肿瘤药物前体:合成血卟啉类抗肿瘤药(如FDA批准的氯化血红素)。
-
抗氧化与免疫调节:中和自由基,增强免疫力,辅助改善慢性病。
2. 食品工业
-
人造肉的应用:血红素精准结合植物蛋白,赋予人造肉逼真的色泽、风味与质地,降低致癌风险。
-
营养强化剂:补充铁元素,提升食品营养价值。
3. 农业与化工
-
植物生长调节剂: 促进光合作用,增强抗逆性,提高作物产量和品质。
-
生物源杀菌剂: 部分含血红素组合物可防治作物病害,减少化学农药使用。
-
生物催化平台: 用于高选择性不对称合成(药物/材料)及构建具有酶活性的功能材料,推动绿色合成工艺。
血红素合成的局限性与挑战
传统方法弊端显著
-
化学合成与天然提取法:产品纯度低、副产物多、环境污染大。
-
高附加值衍生物提取:天然含量极低,导致成本高昂且无法满足市场需求。
生物合成瓶颈
-
产量低下: 现有微生物工程菌株的血红素产量普遍低于300 mg/L,其衍生物(如胆红素)产量甚至不足20 mg/L。
-
成本过高: 生产过程严重依赖添加昂贵中间体(如谷氨酸、甘氨酸、琥珀酸),推高成本,阻碍工业化应用。
-
代谢通量失衡: 以葡萄糖/甘油为原料时,合成路径中关键基因表达不协调,导致代谢流在中间步骤受阻(“堵车”效应),限制了终产物的高效合成。
因此,亟需开发一种高效、安全且经济的血红素生物合成策略,通过优化多酶复合体结构、提升基因表达效率及调控宿主代谢,实现血红素的规模化绿色生产。
微生物合成血红素研究进展
目前已经有大量的通过代谢工程改造进行微生物合成血红素及其衍生物的工作。虽具高效底物通道化、低副产物等理论优势,但酶催化效率低、前体代谢物被竞争消耗、外源酶在宿主中表达障碍等问题还有待解决。
2025年6月,吉林大学与江南大学联合研究团队在国际权威期刊《Journal of Agricultural and Food Chemistry》 上发表重要研究成果[1]。团队提出了“定制化迭代模块代谢通量分析(CIM-MFA)”策略,将复杂的血红素合成通路分解为三个关键模块进行系统性优化,成功构建了具有强大内源血红素供应能力的谷氨酸棒杆菌工程菌株HEME3-ΔhrtBA,其血红素产量较野生型提高了90.75倍。在摇瓶水平即实现了四种重要血红蛋白和肌红蛋白的克级每升高产,创造了该类蛋白微生物合成的新纪录。

泓迅生物解决方案
尽管谷氨酸棒杆菌工程化改造在血红素合成路径优化上取得了显著进展,但还需要面向大规模工业化生产。泓迅生物通过将多酶复合体设计、AI驱动的密码子优化以及宿主代谢工程改造三者协同整合,实现了血红素产量的颠覆性提升。
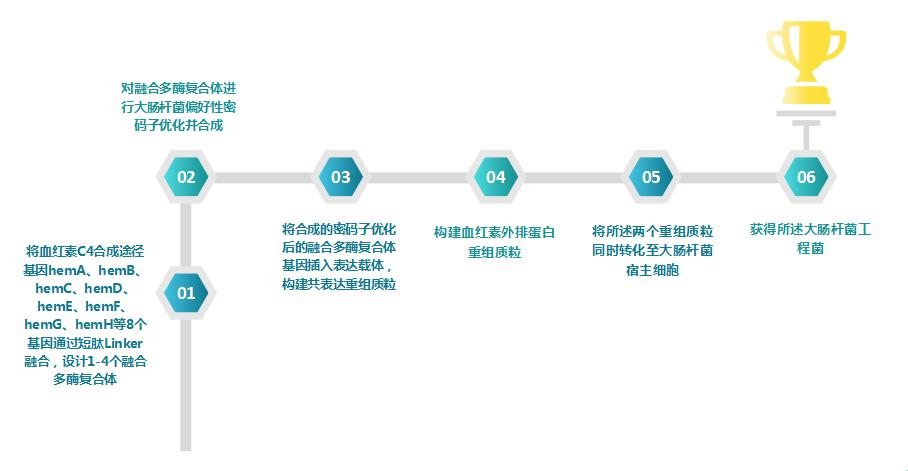
技术路线
采用多酶复合体设计:通过融合多酶复合体设计构建血红素C4合成途径融合多酶复合体实现血红素的高效合成。
AI密码子优化技术(NG Codon 2.0平台):对构建的融合多酶复合体进行深度优化,确保这些复杂且超大分子量的酶组件能在宿主大肠杆菌细胞中实现高效、可溶性的表达,成功突破了传统表达系统在承载大分子量蛋白复合体上的极限。

当血红素合成不再受制于自然提取的局限与化学合成的污染,当每一克产品都源于可再生的葡萄糖与精密的细胞工厂,绿色、高效、可负担的血红素智造,将成为撬动万亿级可持续食品等领域市场的核心支点。
泓迅生物——高效生物分子制造平台
泓迅生物提供先进的人工多酶复合体技术平台及密码子优化平台,为高效生物合成提供核心驱动力。该整合平台不仅成功应用于血红素的高效、高产生物合成,显著提升生产效率和产量,更能灵活拓展至其他高附加值天然产物、精细化学品及生物基材料的合成领域。泓迅生物的合作模式灵活多样,致力于为合作伙伴提供从研发到生产的全方位、定制化解决方案。
合作模式

为什么选择泓迅
泓迅生物依托于AI赋能的生物智能分析专利技术,以及近百亿碱基合成经验,为您提供从基因合成、载体构建到蛋白质表达和纯化的一站式服务。
领先的技术优势—AI密码子优化分析(专利技术)
成熟的蛋白表达经验——四大蛋白表达系统,自主研发数十种高效表达载体
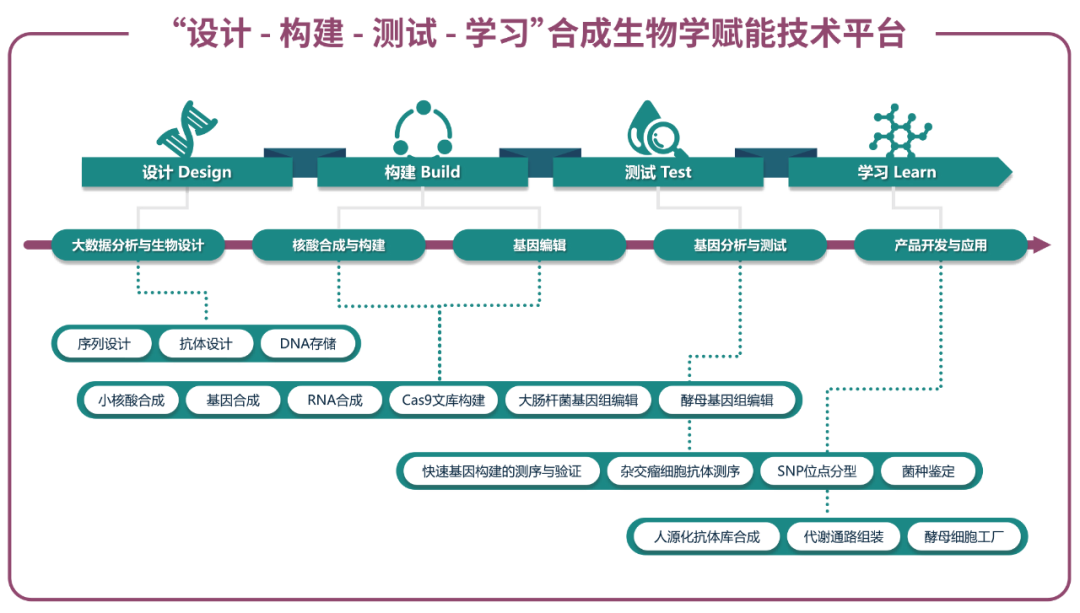
更高的价值服务—一站式合成生物学解决方案
 Syno®C 引物合成
Syno®C 引物合成 RNA合成
RNA合成 mRNA合成
mRNA合成 Syno®GS 基因合成
Syno®GS 基因合成 载体构建
载体构建 高通量及DNA文库构建
高通量及DNA文库构建 CRISPR基因编辑平台
CRISPR基因编辑平台 病毒包装
病毒包装 基因测序与组学分析
基因测序与组学分析 重组蛋白表达平台
重组蛋白表达平台 抗体工程平台
抗体工程平台 多肽服务
多肽服务 生物信息学分析与设计
生物信息学分析与设计 CRISPR文库
CRISPR文库 合成生物学产品
合成生物学产品 ProXpress蛋白快速检测
ProXpress蛋白快速检测 CRISPR 质粒
CRISPR 质粒





















