合成生物学底盘细胞新锐之谷氨酸棒杆菌
谷氨酸棒杆菌(Corynebacterium glutamicum)是一种革兰氏阳性、非致病性的工业微生物,自1957年日本科学家发现其高产L-谷氨酸特性以来,已成为全球氨基酸工业的核心生产菌种。该菌株具备优化的代谢网络和稳定的遗传背景,基因组大小为3.3 Mb。在合成生物学技术的突破下,谷氨酸棒杆菌的应用领域从传统氨基酸生产扩展至重组蛋白表达、生物材料合成等多个高附加值领域,逐渐成为新型蛋白表达底盘的热门候选。
六大核心优势VS 四大技术挑战
为何选择谷氨酸棒杆菌?
- 高效分泌能力:天然具备Sec和Tat分泌途径,S层蛋白(S-layer)的分泌效率显著,胞外蛋白纯度可达90%以上,大大简化下游纯化流程;
- 低内源蛋白酶活性:胞内蛋白酶活性仅为枯草芽孢杆菌的1/5,显著提升外源蛋白稳定性;
- 工业级耐受:耐受pH 5-9、温度(30-42℃)、高渗透压(1.5 M NaCl),适配规模化发酵条件;
- 生物安全:已获美国FDA GRAS认证,适用于食品级和药用蛋白生产;
- 高产潜力:某兽用疫苗抗原产量可达1010 mg/L(远高于大肠杆菌62 mg/L);
- 代谢特性优异:具备广泛的碳源利用谱(葡萄糖、木糖等),并且对营养需求简单。
- 宿主适配性障碍
- 工具元件匮乏
- 生物膜形成倾向
- 基因编辑效率限制
- 宿主限制性屏障:厚肽聚糖细胞壁导致DNA导入效率低下,需优化电穿孔参数。
- 动态调控工具缺乏:代谢通路精细调控依赖外源诱导系统(如IPTG),增加工业化成本。
- 基因组注释空白:约43%基因功能尚未明确(KEGG数据库统计),限制理性设计能力。
- 新型编辑工具开发
- 人工智能辅助设计
- 动态调控系统构建
- 工业适配性改造
技术瓶颈如何突破?
外源基因的表达需要对宿主系统进行系统性优化,像密码子偏好性调整、mRNA二级结构预测等,开发周期较传统系统长出30-50%。
可用的启动子不足20种,信号肽库仅覆盖30%的分泌蛋白类型,限制了在特定应用中的扩展性。
在工业化发酵过程中,易形成生物膜,导致传质效率下降10-15%。
电转化效率普遍低于10⁶ CFU/μg DNA,多位点编辑的成功率不足5%,限制了基因组改造的效率和范围。
基因编辑技术:效率革命进行时
|
编辑方法 |
编辑效率 |
应用场景 |
技术局限 |
|---|---|---|---|
|
自杀质粒同源重组 |
0.1-1% |
单基因敲除/标记删除 |
假阳性率高(>15%) |
|
Cre/loxP重组系统 |
30-50% |
无痕编辑/基因插入 |
需预置loxP位点 |
|
CRISPR-Cas9 |
70-90% |
精准敲除/多基因编辑 |
脱靶率0.5-2% |
|
CRISPR-Cpf1 |
80-95% |
AT-rich区域编辑 |
PAM序列限制(TTTN) |
现存挑战
泓迅生物改造案例
泓迅生物科技采用 CRISPR-Cpf1 系统,在ATCC 13032基因组实现 2.3 kb 双基因表达盒的高效整合(图1)。通过改造编辑质粒、优化sgRNA二级结构及HDR模板设计,整合效率达78%,较传统方法提升数倍。
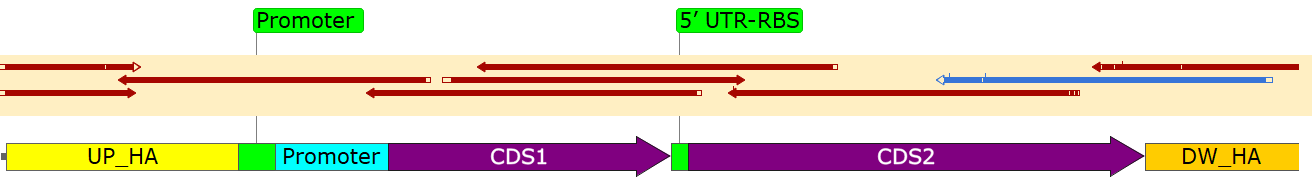
图1
谷氨酸棒杆菌正从“传统氨基酸工厂”进化为合成生物学超级底盘,而基因编辑效率与工具短板仍是产业化拦路虎。泓迅生物深耕合成生物学十年,拥有丰富的基因合成、蛋白表达和基因编辑经验。以微生物基因编辑技术+AI设计为核心,提供一站式解决方案,帮助解决谷氨酸棒杆菌载体构建和基因编辑的需求,助力客户突破技术瓶颈,加速生物制造产业化进程。
限时福利

*仅限前20位
未来发展:AI+合成生物学双引擎驱动
探索微型Cas蛋白(如Cas12f,仅700 aa)及非经典PAM识别系统,突破现有序列限制,提高基因编辑的灵活性与效率。
应用深度学习算法(如AlphaFuld2)预测宿主-外源蛋白互作,优化密码子使用偏好性,为蛋白表达系统的构建提供智能化支持。
开发代谢物感应开关(如赖氨酸响应型启动子),实现产品合成的自主反馈调控,进一步提高产物的生产效率。
通过实验室自适应进化(ALE)选育高产量、抗噬菌体、抗剪切力等工业菌株,提升菌株的工业应用性能。
 Syno®C 引物合成
Syno®C 引物合成 RNA合成
RNA合成 mRNA合成
mRNA合成 Syno®GS 基因合成
Syno®GS 基因合成 载体构建
载体构建 高通量及DNA文库构建
高通量及DNA文库构建 CRISPR基因编辑平台
CRISPR基因编辑平台 病毒包装
病毒包装 基因测序与组学分析
基因测序与组学分析 重组蛋白表达平台
重组蛋白表达平台 抗体工程平台
抗体工程平台 多肽服务
多肽服务 生物信息学分析与设计
生物信息学分析与设计 CRISPR文库
CRISPR文库 合成生物学产品
合成生物学产品 ProXpress蛋白快速检测
ProXpress蛋白快速检测 CRISPR 质粒
CRISPR 质粒





















